Diagnose
Verdenking op amyloïdose
Het opsporen en vaststellen van de aanwezigheid van amyloïd wordt voorafgegaan door het ontstaan van een klinische verdenking op amyloïdose, zie Tabel. Klinische verdenking op amyloïdose kan ontstaan op velerlei manieren.
| Categorie | Klinische situatie | Ziekteverschijnselen | Type amyloïd | Voorkeursplek biopsie |
| I | Onverwacht en onverklaard of bij mensen met een al bekende plasmacel dyscrasie |
Proteïnurie, nierfunctieverlies, diarree, organomegalie (lever, milt of tong), hartfalen, biventriculair verdikte hartwanden, ritme- of geleidingsstoornissen, orthostatische hypotensie, perifere axonale polyneuropathie, autonome neuropathie, carpaletunnelsyndroom, ernstig gewichtsverlies of malabsorptie | AL | Eerste: buikvet#; Tweede: ziek weefsel& | II | Bekend met lang bestaande ontsteking | Proteïnurie, nierfunctieverlies, hartfalen, diarree, hepatomegalie of splenomegalie | AA | Eerste: buikvet#; Tweede: ziek weefsel& |
| III | Behorend tot een familie met een erfelijke amyloïdose | Ziekteverschijnselen behorend bij dat specifieke type amyloïdose. Enkele voorbeelden: Cardiomyopathie in ATTRv, Nefropathie in AFib en Cornea lattice dystrofie in AGel | Erfelijke typen, zoals ATTRv, AApoAI, AFib, AGel, en andere* | Eerste: buikvet#; Tweede: ziek weefsel& | IV | Een oudere, vaak mannelijke patiënt zonder cardiovasculaire voorgeschiedenis | Hartfalen bekend met een carpaletunnelsyndroom, boezemfibrilleren, aorta stenose, of spinale stenose | ATTRwt | Endomyocard of botscan$ |
| V | Een tumor op een specifieke plek van het lichaam | Larynx of bronchiaal boom, urogenitale tractus, ooglid, maagdarmkanaal, farynx | AL lokaal | Ziek weefsel | VI | Eosinofiel materiaal in een biopsie: amyloïd aanwezig? | Tevoren niet als zodanig herkend door de aanvragende arts. Een alerte, meedenkende patholoog | Alle typen | NA |
#Algemeen, maar in sommige centra kiest men als eerste voor de lipspeekselklier of het rectum.
&Rectum, maagdarm (niet gespecificeerd) of lip kunnen eventueel als alternatief of tussenstap.
*Zie: Benson M. et al. Amyloid nomenclature 2020. Amyloid 2020; 27:217-22.
$Wanneer AL-amyloïdose is uitgesloten door een negatieve IFE van het serum en urine en bij normale immunoglobuline vrije lichte ketens in het bloed.
NA, not applicable.
Een eerste categorie bestaat uit de mensen die nieuwe symptomen of andere ziekteverschijnselen hebben ontwikkeld die niet passen bij hun medische voorgeschiedenis. Ook door een onbegrepen vergroting van tong, lever of milt, bij een gestoorde werking van zenuwen (neuropathie) aan beide benen, ernstig verlies van eiwit via de nieren of nierfalen, ernstige diarree, of hartfalen met sterk verdikte hartwanden kan soms de verdenking op amyloïdose ontstaan. De verdenking neemt toe bij meer dan één ziekteverschijnsel.
Een tweede categorie bestaat uit patiënten met een lang bestaand ontstekingsbeeld, zoals reumatoïde artritis. Dan is het goed om op de eventuele ontwikkeling van AA-amyloïdose bedacht te zijn door regelmatig de urine op de aanwezigheid van eiwit te controleren en de nierfunctie goed in de gaten te houden.
Een derde categorie bestaat uit leden van een familie waarin erfelijke amyloïdose voorkomt en bij wie verschijnselen zijn ontstaan die passen bij dat type amyloïdose.
Een vierde categorie bestaat uit oudere (veelal mannelijke) patiënten met hartfalen zonder een cardiovasculaire voorgeschiedenis, maar met wel een ander kenmerkend verhaal.
Een vijfde categorie bestaat uit patiënten met een of meer zwellingen die gelokaliseerd zijn op specifieke plaatsen van het lichaam.
De laatste, maar niet de minst frequente categorie, bestaat uit mensen bij wie de amyloïdose ontdekt wordt door een alerte patholoog. Na het vinden van verdacht eosinofiel materiaal in een weefselbiopsie besluit deze om alsnog een kleuring met Congo rood te verrichten resulterend in het vinden van amyloïd.
Verdenking alleen is onvoldoende, de aanwezigheid van amyloïd dient ondubbelzinnig te worden vastgesteld in een stukje weefsel, een zogeheten biopt.
Vaak is de uitslag van zo’n biopt de eerste bevinding dat er sprake is van amyloïdose. Door de relatieve zeldzaamheid van amyloïdose, de sterk verschillende wijzen waarop de ziekte zich kan presenteren en het verraderlijke en zeer geleidelijke ontstaan van ziekteverschijnselen wordt de ziekte in veel gevallen pas ontdekt in een laat stadium, waarin al ernstige schade is toegebracht aan één of meer organen.
Verdere evaluatie in het kort
Na het vinden van amyloïd in een stukje weefsel behoort nader onderzoek plaats te vinden door het typeren en in kaart brengen van de ernst en uitgebreidheid van de amyloïdose. Belangrijk is of het amyloïd lokaal of systemisch gestapeld wordt en welke organen en weefsels bij deze stapeling betrokken en eventueel beschadigd zijn. Hierdoor ontstaat een beeld van de ernst en uitgebreidheid van de amyloïdose en kan een globale inschatting van de prognose worden gemaakt. Uitgaande van deze situatie dient gekeken te worden of er mogelijkheden tot behandeling bestaan en zo ja welke mogelijkheden dat zijn.
Biopt
Om de aanwezigheid van amyloïd vast te stellen, is het vereist om dit in weefselcoupes aan te tonen. Dit kan door een positieve aankleuring met Congorood met de daarbij typische appelgroene dubbelbreking in gepolariseerd licht. Voor dit doel is de buikvetbiopsie de meest elegante en minst belastende methode, met een vangkans van >90% bij de meeste vormen van systemische amyloïdose als de biopsie en de verwerking daarvan goed wordt uitgevoerd. Een goed alternatief is het onderzoeken van een rectumbiopt. Bij een negatieve uitslag van één van deze twee methoden en toch sterke verdenking op amyloïd is het zinvol om ook de andere methode toe te passen (of de wat minder vaak positieve beenmergbiopsie). Als echter alle biopten negatief zijn en de verdenking op amyloïd groot blijft, dan is een biopsie van het verdachte orgaan of weefsel aangewezen.
Hieronder voorbeelden van de Congorood kleuring van geaspireerd vetweefsel. Dit weefsel kan poliklinisch worden afgenomen onder plaatselijke verdoving, iets naast de navel en vlak onder de buikhuid. Download hier de instructie video (ongeveer 15 MB) en bekijk de Vet aspiratie procedure 2019 (pdf bestand) voor meer details.
 |
 |
Vetaspiraat – normaal licht | Vetaspiraat – gepolariseerd licht |
Zoals zichtbaar in de bovenstaande figuren is het amyloïd in het vetweefsel herkenbaar als roodgekleurde afzettingen tussen de normale, iets blauw gekleurde architectuur van vetweefsel. Wanneer het bekeken wordt in gepolariseerd licht verandert de rode kleur in groen of groengeel. Deze groene dubbelbreking van met Congorood gekleurd materiaal in gepolariseerd licht is kenmerkend voor amyloïd.
In het laboratorium kan vervolgens het amyloïd uit het biopt geëxtraheerd worden en naar de aanwezigheid en hoeveelheid van voorlopereiwitten, de zogeheten precursors, gekeken worden. Ook kan onder de microscoop in weefselcoupes van het aangedane orgaan gekeken worden met specifieke antilichamen (gericht tegen de voorlopereiwitten) om de aanwezigheid van amyloïd onomstotelijk vast te stellen en te onderzoeken welk type amyloïd het betreft.
Typering
Klinische inschatting van het type amyloïd
Na bevestiging van de aanwezigheid van amyloïd in weefsel moet typering volgen. In veel gevallen kan op grond van voorgeschiedenis, klachten en klinisch beeld al een goede inschatting worden gemaakt van het type amyloïd. Een patiënt met lang bestaande reumatoïde artritis en een nefrotisch syndroom heeft zo goed als zeker het AA-type. Iemand met polyneuropathie die behoort tot een familie met erfelijk amyloïd zal waarschijnlijk het ATTR-type hebben. En bij een patiënt met de karakteristieke “shoulder pads” en een sterk vergrote tong staat het AL-type bovenaan. Ook bloed-, urine- en beenmergonderzoek kan helpen bij het inschatten van welk type amyloïdose sprake is. Bij AL-amyloïdose kunnen in veel gevallen vrije lichte ketens worden aangetoond in het bloed en/of de urine. In het beenmerg kunnen klonale plasmacellen worden aangetoond. Bij AA-amyloïdose kunnen verhoogde acute fase eiwitten (zoals CRP en het precursor eiwit SAA) in het bloed worden gevonden. Dit is illustratief maar zeker niet bewijzend voor AA-amyloïdose omdat deze ontstekingseiwitten bij heel veel andere aandoeningen ook verhoogd in het bloed aanwezig kunnen zijn.
Ook al is een bepaald type amyloïd klinisch aannemelijk, toch is een bevestiging van het type amyloïd noodzakelijk voor het verdere beleid. De wijze van behandeling van de verschillende systemische typen loopt namelijk sterk uiteen.
Typering met behulp van het biopt
Immunohistologisch onderzoek van het biopt biedt de mogelijkheid om het type amyloïd via specifiek gerichte antilichamen nader te karakteriseren. Bij AA-amyloïdose is dit onderzoek toereikend voor de typering, mits hiervoor sensitieve en specifieke monoklonale antilichamen worden gebruikt. Echter bij AL- en ATTR-amyloïdose schiet deze methode in sommige gevallen tekort omdat de gebruikte antilichamen minder specifiek zijn en de antigene herkenbaarheid van het precursoreiwit binnen de amyloïdafzettingen verminderd is.
Hieronder zijn voorbeelden te zien van een nierbiopt van een AA-amyloïdose patiënt waar links het biopt gekleurd is met Congorood (waar het effect van het polarisatiefilter is te zien) en rechts de Immunohistochemische kleuring met het specifieke monoklonale antilichaam gericht tegen Serum amyloïd A (SAA; clone Reu86.2).
 |
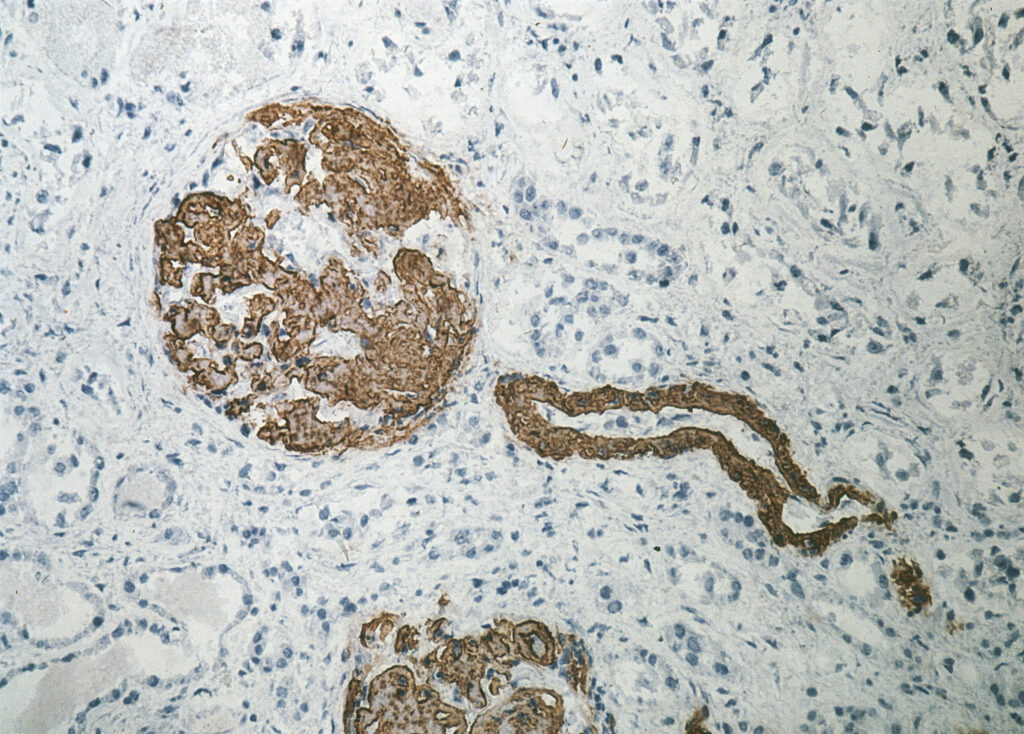 |
Nier – Congorood kleuring | Nier – Immunohistochemie kleuring met anti-SAA |
In Groningen hebben we de mogelijkheid om uit het buikvetbiopt het amyloïd te extraheren en middels een panel van immunochemische testen, zogenaamde ELISA’s, het amyloïd nader te typeren. Deze methode is geschikt om de meest voorkomende typen amyloïdose (AA, AL-kappa, AL-lambda en ATTR) van elkaar te onderscheiden, maar werkt alleen als er voldoende amyloïd in het vetbiopt aanwezig is. Indien het met deze methode niet lukt om het amyloïd te typeren, kan gebruik worden gemaakt van andere biochemische technieken zoals massaspectrometrie (proteomics).
Genetisch onderzoek
Indien er sprake blijkt van ATTR amyloïdose, zal met DNA-onderzoek onderscheid gemaakt worden tussen de erfelijke en de wild-type vorm. Naast erfelijke ATTR-amyloïdose zijn er verschillende andere, zeldzamere typen erfelijke amyloïdose (zie tabel).
Het DNA-onderzoek gebeurt bij de afdeling Klinische Genetica. De meeste vormen van erfelijke amyloïdose hebben een autosomaal dominant overervingspatroon.
Wanneer erfelijke amyloïdose wordt vastgesteld, komen volwassen familieleden in aanmerking voor DNA-onderzoek. Patiënten met erfelijke amyloïdose ontvangen hiervoor een informatiebrief die zij aan hun familieleden kunnen geven. Familieleden die DNA-onderzoek naar erfelijke amyloïdose wensen en/of hier meer informatie over willen, kunnen door hun huisarts naar de afdeling Klinische Genetica verwezen worden. Als uit DNA-onderzoek blijkt dat iemand drager is van de aanleg voor erfelijke amyloïdose, volgt een verwijzing naar het expertisecentrum voor screening op eventuele verschijnselen.
| Afkorting | Eiwit (precursor) |
Aangedane organen |
| ApoAI | Apolipoproteïne A-I | Hart, lever, nieren, zenuwen, larynx |
| ApoAII | Apolipoproteïne A-II | Nieren, hart |
| ApoCII | Apolipoproteïne C-II | Nieren |
| ApoCIII | Apolipoproteïne C-III | Nieren |
| Beta2M | Beta-2 microglobuline | Maag- darmstelsel, autonoom zenuwstelsel, speeksel- en traanklieren |
| CST3 | Cystatine | Hersenen |
| FGA | Fibrinogeen Alfa keten | Nieren |
| GSN | Gelsolin | Zenuwstelsel, huid en ogen |
| IL31RA | Interleukin-31 receptor A | Huid |
| LYS | Lysozyme | Nieren, lever, hart, milt, maag- darmstelsel, speekselklieren |
| OSMR | Oncostatin M receptor | Huid |
| TTR | Transthyretine | Zenuwstelsel, hart, ogen, hersenvliezen |
In het kort
- Als er verdenking bestaat op amyloïdose, moet het amyloïd worden aangetoond in een biopt
- Ook moet het type amyloïd worden vastgesteld. Hiervoor zijn verschillende laboratoriumtechnieken beschikbaar
- Om te beoordelen of er sprake is van een erfelijke vorm van amyloïdose, wordt genetisch onderzoek gedaan.

